Le contrôle de qualité des dispositifs médicaux est l’ensemble des opérations destinées à évaluer le maintien des performances revendiquées par le fabricant ou le cas échéant, fixées par des décisions du directeur général de l’Agence nationale de sécurité du médicament et des produits de santé (ANSM). Les décisions du directeur général de l’ANSM définissent des modalités particulières de contrôle pour chaque type de dispositif médical. Les décisions actuellement en vigueur portent sur les dispositifs médicaux exposant les personnes aux rayonnements ionisants, elles fixent notamment la nature, la périodicité et les critères d’acceptabilité des contrôles à réaliser.
Le contrôle de qualité est dit interne, s’il est réalisé par l’exploitant ou sous sa responsabilité par un prestataire. Il est dit externe, s’il est réalisé par un organisme indépendant de l’exploitant, du fabricant et de celui qui assure la maintenance du dispositif. Ces organismes indépendants, appelés organismes de contrôle de qualité externe (OCQE), demandent un agrément auprès de l’ANSM pour être en mesure de réaliser les contrôles de qualité dans nos cabinets. La liste des organismes de contrôles de qualité externe par agrément est disponible sur le site de l’ANSM.
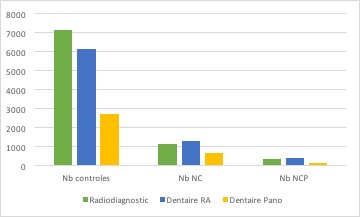
Les contrôles de qualité internes et externes permettent de constater des non-conformités. Si ces non-conformités sont graves ou persistantes, elles doivent être signalées à l’ANSM. Les non-conformités graves nécessitent l’arrêt d’utilisation de l’installation jusqu’à remise en conformité. Les non-conformités persistantes sont des non-conformités mineures n’ayant pas fait l’objet d’une remise en conformité avant le contrôle suivant.
